Fig. 3-1 Absorption : les rayons X sont atténués lorsqu'ils pénètrent dans la matière, ceci dépend entres autres de la longueur d'onde
| précédent |
| Introduction | Principes physiques | * | Les spectromètres | Mise en équation des effets de matrice | Bibliographie et liens |
3 -- Les effets de matrice
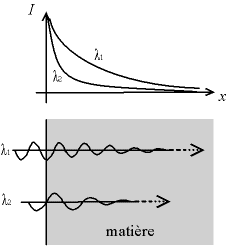
Les rayons X sont absorbés par la matière. Quand les rayons X pénètrent dans l'échantillon, ils sont atténués, essentiellement absorbés par effet photoélectrique. L'absorption dépend de la nature de l'échantillon :

Fig. 3-1 Absorption : les rayons X sont atténués
lorsqu'ils pénètrent dans la matière,
ceci dépend entres autres de la longueur d'onde
C'est ce qui est exploité pour les radiographies médicales : les rayons X sont plus absorbés par les os (denses et contenant des éléments lourds comme le calcium Ca) que par la chair et les organes mous (peu denses et composés d'éléments légers comme le carbone C, l'hydrogène H, l'oxygène O, l'azote N).
Donc, si l'on a de l'eau contenant 10 ppm de plomb en masse (c.-à-d. 1 mg de plomb par kg d'eau), et une roche contenant elle aussi 10 ppm de plomb en masse, l'intensité de la raie du plomb sera plus grande pour l'échantillon aqueux que pour la roche, car moins absorbé.
| début |
Les photons fluorescents peuvent à leur tour provoquer une excitation des atomes voisins, et donc de la fluorescence. On parle de «fluorescence secondaire» ou de «surexcitation« (enhancement).
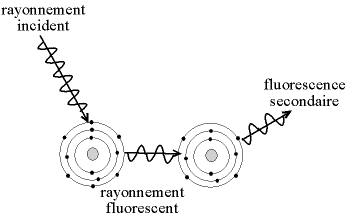
Fig. 3-2 Fluorescence secondaire
| début |
Les éléments légers (faible numéro atomique) ne sont pas mesurables par fluorescence X, et ce pour deux raisons :
Les échantillons géologiques et cimentiers sont souvent formés d'oxydes, carbonates, de produits hydratés...
Même si l'on ne s'intéresse pas aux teneurs en C, H, O... il faut quand même les connaître, car ils ont une influence capitale sur les effets de matrice. Trois approches sont possibles.
Supposons que l'on soit sűr que l'aluminium soit présent sous forme d'oxyde Al2O3 (alumine). Alors, on peut dire : «chaque fois que je compte deux atomes d'aluminium, je rajoute trois atomes d'oxygène». C'est ainsi que par abus de langage, on dit souvent que l'on "mesure la teneur en oxyde" ; en fait, on mesure la teneur en aluminium, et on en déduit la teneur en oxyde par stoechiométrie.
L'approche stoechiométrique est très souvent utilisée en contrôle de production, où l'on sait souvent sous quelle forme chimique se trouvent les éléments, ainsi qu'en géologie.
Cependant, cela n'est pas possible si l'on ne connaît pas la forme chimique, ou bien si un élément est présent sous plusieurs formes, par exemple si l'on a plusieurs oxydes de fer (FeO, Fe2O3, Fe3O4).
Ce calcul est fait directement par le logiciel de traitement.
Si l'échantillon comporte un composé chimique dont aucun des éléments n'est mesurable, comme par exemple l'eau H2O (échantillon hydraté), l'huile... on peut tout simplement dire qu'il constitue toute la masse manquante : on fait la somme des concentrations calculées, et l'on déclare que le complément à 100 % de cette somme est fait dudit composé
Ce calcul est fait directement par le logiciel de traitement.
La dernière solution consiste à utiliser d'autres méthodes d'analyse pour mesurer les éléments légers, et d'en déclarer la teneur au logiciel de traitement afin qu'il puisse les prendre en compte pour les corrections de matrice.